即可将网页分享至朋友圈
头颈部癌症是一个冷酷的杀手,以其极高的发病率和致死率令人闻之色变。所幸人类有“精准放疗”这个法宝,使它不能恣意妄为。然而,“道高一尺,魔高一丈”,头颈癌藏身之处是人体极为关键的部位,有腮腺、脑干等重要组织器官,而目前放疗的精度并不能完全保证射线不伤及无辜,因此“精确放疗”虽然武艺高强,但在实际操作中依然投鼠忌器、束手束脚。
究竟如何对头颈癌实施精准打击呢?近日,自动化工程学院成像科学与图像处理研究中心王振松博士在国际图像处理领域著名期刊《IEEE Transactions on Image Processing》发表研究论文,提出了一种智能化、精准化的图像分割新方法,以辅助医生精确勾画头颈部组织器官的解剖位置,为放疗打靶头颈部肿瘤提供“精确制导”。
论文截图
这篇论文题为“Hierarchical Vertex Regression-based Segmentation of Head and Neck CT Images for Radiotherapy Planning”,被该期刊选为2018年2月的封面论文。王振松博士为论文第一作者,美国北卡罗莱纳大学教堂山分校沈定刚教授为通讯作者,电子科技大学为第一作者单位。

《IEEE Transactions on Image Processing》封面
“精确打靶”:放疗呼唤火眼“精”睛
放疗是临床治疗头颈癌的主要方法之一。随着技术的进步,人类已经能够对放疗的辐射剂量进行精确控制和精准投送。相对来说,对靶区的精确勾画技术还不能满足日益增长的临床需求。这就导致了即便放疗的“枪法”很准,但如果“敌我难分”,也有可能对病人的正常器官造成严重“误伤”。
即便找到了靶区,要做到十分精准,依然任重道远。如果靶区小于肿瘤的实际体积,则无法彻底清除癌细胞,可能导致癌细胞残留或癌症复发;如果靶区大于肿瘤的实际体积,则会造成杀伤范围过大,伤及无辜的正常组织或器官。因此,医生在三维CT图像上勾画肿瘤靶区时十分小心。
目前常用的CT影像是断层切片扫描的黑白影像,医生在每一个切片影像上手动勾画靶区,然后叠加起来确定三维靶区的位置。切片越多越密,三维靶区的精度越高。然而,如果切片过多,医生手动勾画靶区的工作量就会非常大,而且工作十分枯燥、效率低下;如果减少切片,又会降低靶区勾画的精度。
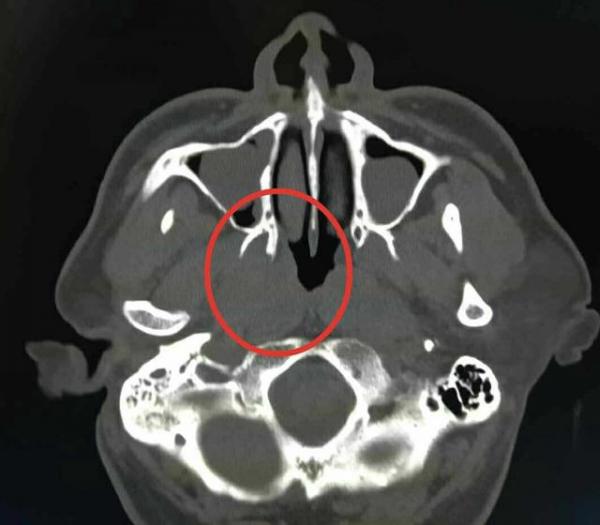
图为常见的头颈部CT影像,由从黑到白的不同灰度的象素构成
“在技术层面,我们可以把影像切片的间距控制在1毫米以内,但要人工勾画这么多片子,医生会很累,而且会耗费许多时间。”王振松说,头颈部的器官非常小,而且非常多。据文献记载,有经验的医师手动完成一例头颈部放疗计划的勾画平均耗时2.7个小时。
于是,如何进一步提升靶区和重要器官勾画的精度,同时把医生从繁重的手动勾画工作中解放出来,成了治疗头颈癌的重要临床需求。与之相对应,如何把先进的医学影像技术和百年来临床放射治疗癌症的知识和经验进行整合优化,实现半自动或全自动的癌症(或肿瘤)靶区精准勾画,成为了当前医学图像处理领域的研究热点。
创新算法:实现智能精准识别
在王振松之前,学界已经探索出了“基于图像灰度表观特征的多图谱分割方法”、“基于形状模型的分割方法”等勾画头颈癌靶区的方法。这些方法在勾画靶区时均有所侧重,有的基于灰度,有的基于形状模型,有的基于图谱,每种方法各有所长,但也各有所短。因此,他意识到,靶区勾画方法可能呼唤新的交叉或综合。
以基于灰度的方法为例,王振松说,“计算机可以帮助医生区分CT影像中人眼无法识别的细微灰度变化,但头颈部的软组织在CT图像上的灰度分辨率很低,即便是计算机也很难精准区分,误差较大。而且,如果遇到金属植入物干扰,比如金属假牙在CT成像中会产生一块伪影,导致靶区勾画更加困难。”
难道鱼与熊掌真的不能兼得吗?能否把这些方法综合起来,各取所长、相互印证,进一步提升勾画的准确度呢?王振松的思路是,把图谱和形状综合起来,提出一种“多级学习模型”,先让计算机“学习”大量的图谱,这些图谱都是由医生手工勾画并经过临床检验的,“先验”地掌握头颈部器官或组织的分布规律。
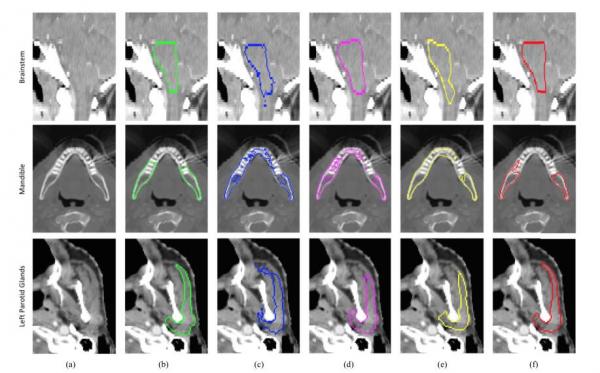
(图为不同方法分割结果的视觉效果比较。第1行是包含脑干的失状面CT成像切面;第2行是包含下颌骨的轴向CT成像切面;第3行是包含左腮腺的轴向CT成像切面。每行的6列分别为原始CT影像以及五种分割后的结果轮廓,不同颜色表示不同方法的分割结果:(a)原始CT影像;(b)绿色-目标器官的真实轮廓;(c)蓝色-基于灰度图像表观方法的分割结果;(d)粉色-传统的形状模型方法的分割结果;(e)黄色-等权重顶点回归方法的分割结果;(f)红色-王振松提出的多级顶点回归方法的分割结果。可以看出,(f)图勾画的结果最接近(b)图的器官真实轮廓)
然后,计算机又结合基于解剖学的“组织器官”的形状等先验知识,按照知识关键性进行同步逐级学习。在此过程中,该方法建立了“形状顶点关键度评判”新机制,提出了“多级形状顶点回归”新策略,构建了“形状和图像表观联合学习”新框架。“这个方法可以很好地解决金属假牙造成的干扰,这是单纯地基于灰度的方法难以解决的问题。”
通过比较,他提出的“多级顶点回归方法”的分割结果最接近目标器官的真实轮廓。实验数据显示:在勾画脑干时,其他5种方法的DSC值(Dice Similarity Coefficient,即一种相似性测度,数值越高意味着越相似、越准确)分别为88±3%、86±5%、85±5%、80±7%、86±(-)%,而王振松的结果是90±4%;在勾画下颌骨时,其他5种方法的DSC值分别为91±2%、93±2%、88±6%、92±2%、79±5%,而王振松的结果是94±1%;在勾画腮腺时,其他5种方法的DSC值分别为82±1%、76±8%、82±5%、81±5%、82±(-)%,而王振松的结果是83±6%。也就是说,他的方法在靶区勾画的精确度上有了大幅提升。
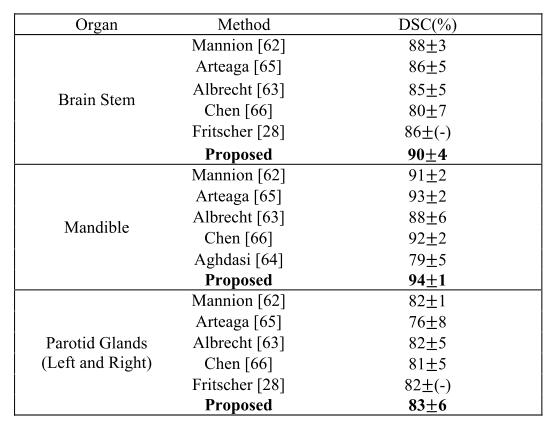
图中第一行为不同方法勾画脑干的结果对比;第二行为勾画颌骨的结果对比;第三行为勾画左右腮腺的结果对比。可以看出,王振松的方法DSC值最高,勾画效果最好。
美好心愿:“信息医学”让医疗更智能
2015年底至2016年底,王振松在美国北卡罗莱纳大学教堂山分校访学时,在沈定刚教授的指导下开始研究头颈部CT图像的处理问题。从接触这个研究方向到最终做出这项成果,他只用了一年时间。
“我刚开始做的是图像配准研究,就是把不同时间、不同传感器或不同条件下获取的图像进行匹配、叠加,这和我现在所做的CT图像分割研究有很大区别,”他说,“沈定刚教授团队有很好的研究基础,因此,我有幸能够站在前人的基础上,取得了这项研究进展。”
与最终发表的论文相比,编算法、写代码是更加艰辛的工作。为了让计算机“学”会如何分割或识别图像,他编写了大量代码,而且要在测试的过程中不断修正,甚至按照新的思路推倒重写。值得庆幸的是,他曾经从事的软件开发工作,为研究的顺利进行奠定了坚实基础。同时硬件条件也很重要,算法执行时要同时调动上百个CPU,每个CPU同时运行至少8个线程,这样才能满足运算需要。
现在,王振松正在进一步优化算法。他说,这种方法是一种很有潜力的方法。在较好的硬件条件下,该算法采用的并行加速技术可以成百倍、上千倍甚至更多倍地缩短靶区勾画的时间。据统计,该方法在64位系统、一个Intel i7-4570 CPU、3.2GHz主频、16G内存的硬件平台上完成一例脑干的分割,耗时仅为36分钟。
然而,要满足临床应用的要求可能还有一定距离。王振松介绍,“我们统计的耗时还不能直接等同于前面所说的医师手动勾画时间,因为我们统计的是对一个器官图像分割的时间,而医生的手动勾画时间是对放疗计划中靶区和所有危及器官图像勾画所耗费的平均时间。但整体来说,自动图像分割技术采用了并行计算等加速技术后,分割速度肯定会比手动勾画快得多。”
目前,他正在努力让算法更精确、更高效,并正在与华西医院、成都市第六人民医院等进行合作。然而,精益求精并不容易,因为当分割精确度越来越趋近于100%的时候,每提高1个百分点甚至0.1个百分点,都需要付出极大的努力。他说,“我有一个心愿,就是让头颈癌靶区勾画越来越精准、越来越智能,既能减轻医生的工作压力,也能为病人带来福祉,为我国的健康事业做出更多贡献。”
编辑:林坤 / 审核:罗莎 / 发布:陈伟


